周更专栏 | 肠道相关免疫系统及其健康影响
结论
越来越多的研究报告指出,肠道及其肠道生态系统对于人类的整体健康(编者加注:包括抗衰老)具有相当大的重要性,胃肠系统的重要性绝不仅仅是一个消化器官。而住在肠道中的人体内最大的微生物群会影响新陈代谢和免疫调节,它们通过提供能量载体或释放免疫调节物质来控制代谢过程,所以肠道菌群最近又被定义为一种代谢器官。
为什么微生物组如此重要
肠道及其定植微生物组是健康生活最重要的先决条件之一。健康生活最重要的系统需求在肠道中得到满足。这些包括免疫系统、神经系统和代谢系统。这些人体大器官系统的紊乱往往会影响肠道健康,甚至起源于肠道,受到肠道内生态平衡的影响。
原书中深入讨论了肠道菌群失调和各种临床症状之间的关系,包括肥胖、代谢综合征、结肠炎、肠道肿瘤、关节炎、自闭症、阿兹海默症等。需要重点支出的是,肠道炎症通常是肠道菌群失衡的结果。大家普遍重视的高度炎症,往往会伴随显著炎症症状(疼痛、粘液分泌、血便等),并且需要紧急医疗干预,但肠道中的低度炎症恰恰是许多慢性疾病的原因。这里只对于衰老关系较大的阿兹海默症做展开,需要进一步了解的,可以从原书中获得。
研究发现,阿尔茨海默症患者的肠道微生物组也发生了变化。几乎 100% 的所有接受测试的阿尔茨海默症患者 (n=52) 的普拉梭菌计数都低。此外,87.5% 的测试者的炎症标志物(钙卫蛋白或抗胰蛋白酶)值升高。 91%的患者的hsCRP值表明体内存在全身炎症。 F. prausnitzii 缺乏会促进肠粘膜炎症。如果能够显着增加A. muciniphila和F. prausnitzii等重要物种的细菌数量,就能达到抗炎和粘膜保护作用。实际上,使用益生元和益生菌制剂治疗就可以促进上述细菌种类的增殖,达成对阿尔茨海默症有利的干预[1]。

我们从粪便菌群分析中可以读到什么
检测人类肠道菌群,首先可以让我们知道肠型(enterotype)。它可以让我们更深入地了解肠道微生物组在人类健康中的意义,目前主要的肠型有三种[2],它们是:
1.拟杆菌型(Bacteroides-type)
2.普雷沃氏菌型(Prevotella-type)
3.瘤胃球菌科型(Rumninococcaceae-type,2016年前称为Rumninococcus-type)
研究表明,这些肠型在个体之间表现出很强的稳定性[3]。分析人类肠道菌群的肠道类型提供了有关特定饮食习惯的信息,并得出如下结论:只有通过长期改变饮食习惯并摄入高比例的特定膳食纤维和益生元才能实现改变。对于日常实践来说,微生物组细菌的分类并不重要。但人们最感兴趣的是某些肠道细菌的代谢性能、微生物组的百分比以及其对健康的支持作用,估计需要首先对粪便样本进行所谓“功能组”的定量分析[4]。
不同肠型可以形成稳定、可清晰区分的细菌簇,具有典型的代谢特性,例如肠型1的主要特征是拟杆菌数量较多,而肠型2的特征是普雷沃氏菌数量较多,肠型3则显示出独特的瘤胃球菌菌群。粪便样本中肠型的规范也可能对维生素和矿物质的吸收产生影响。
微生物组的多样性是粪便菌群分析中另一项结果。它取决于肠道条件,但也可能受到医疗、食物摄入和环境负担等外部因素的影响,如饮食不均衡或频繁服用抗生素会对多样性产生负面影响。超重或患有1型或2型糖尿病、阿尔茨海默症、慢性炎症性肠道疾病、结直肠癌和肠易激综合征的个体在定量微生物组分析中,通常都会表现出多样性降低。
短链脂肪酸(SCFA),有时也会菌群分析中被提及,它对肠道的作用包括:
- 稳定肠道环境(pH值);
- 结肠上皮的能量供应;
- 促进粘蛋白产生;
- 减少炎症;
- 减少细胞增殖;
- 促进细胞凋亡;
- 促进癌细胞分化;
- 基因调控(脱乙酰酶抑制);
- 加强粘膜屏障(减少Claudin‑2 表达);
- 促进调节性T 细胞
基因组测序
近年来,基因组测序对实现特定微生物组的诊断做出了突出贡献。它能在很短时间内达到检测要求,已经覆盖250多个类型和物种,大大超过所有其他方法。基于序列的微生物组分析可以在实验室中轻松并经济地处理粪便样本。借助改进的样品制备和验证程序进行不断优化,以及应用额外的相关指示菌和肠道细菌检测序列,已经成为现代功能性粪便诊断的主要方法[5]。(编者注:2008年启动的“人类微生物组计划”正是依托基因组测序,使得在分子水平上识别和记录人类微生物变为可能,2020-2022年疫情期间,对Covid-19的基因组测序为病毒溯源、疫苗研制、防控政策制定提供了强大支持。)
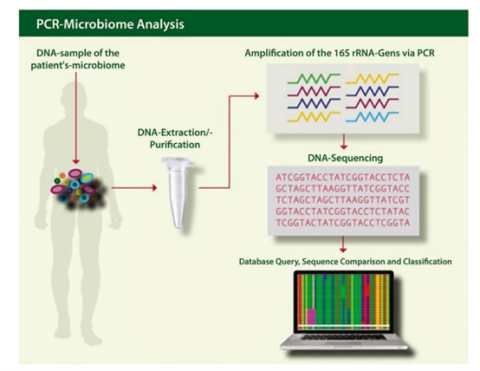
图一:PCR 微生物组分析
1)从患者粪便样本中分离细菌 DNA,并借助 PCR 进行繁殖;2)对目前数量较多的基因片段进行测序,丰富的结果数据通过特殊的计算机程序进行评估;3)基因序列与参考基因组进行比较,以比较、分组细菌。
小结
肠道健康,特别是肠道微生物组多样性,已成为一个突出的问题,在考虑人类健康时至关重要。没有一种人类疾病的存在是不受微生物组的影响或触发的。肠道微生物组与免疫系统、代谢系统和神经系统相互作用。所有这些调节功能都在人类肠道中结合在一起,在实施健康影响过程中需要综合考虑。确定肠道菌群紊乱的精确方法将有助于成功干预。
在过去几十年里,现代肠道治疗中对益生菌和益生元的研究一直进行中。然而,了解某些细菌菌株的功能还有很长的路要走,因为并非所有菌株都具有相同的功能。我们目前认为,保持肠道适宜的状况会为更健康的肠道铺平道路,某些益生元在这里起着决定性的作用。
另外,原书中对比了不同类型的膳食纤维对肠道菌群的作用,还深入讨论了肠漏诊断以及对健康的影响,如肠漏引起的肠道炎症和自身免疫反应。限于篇幅,不做深入展开,欢迎大家阅读原书。
参考文献:
[1] Leblhuber, F. et al.: Elevated fecal calprotectin in patients with Alzheimer’s dementia indicates leaky gut. J Neural Transm (Vienna) 122(9) S. 1319-1322, 2015.
[2] Falony G, Joossens M, Vieira-Silva S, Wang J, Darzi Y, Faust K, Kurilshikov A, Bonder MJ, Valles-Colomer M, VandeputteD, Tito RY, Chaf¬fron S, Rymenans L, Verspecht C, De Sutter L, Lima-Mendez G, D‘hoe K, Jonckheere K, Homo¬la D, Garcia R, Tigchelaar EF, Eeckhaudt L, Fu J, HenckaertsL, Zhernakova A, Wijmenga C, Raes J. Population-level analysis of gut microbiome variation. Science. 2016 Apr 29;352(6285):560– 4.
[3] Stability of Gut Enterotypes in Korean Monozygotic Twins and Their Association with Biomarkers and Diet. Mi Young Lim et al.: Scien¬tific Reports 4, Article number: 7348, Published 12.2014
[4] Mandal, S. et al.: Analysis of composition of microbiomes: a novel method for studying microbial composition. In: MEHD 26, S. 27663- 27670, 2015
[5] Keller, P.M. et al.: 16S-rRNA-Gen-basierte Identifikation bakterieller Infektionen. BIOspektrum S. 755-759, 2010
作者
Claus Muss 教授
华沙预防与健康医学研究所所长
国际实用疾病预防和研究小组主席
解读作者
黄力文 Jason LW. Huang
中国抗衰老临床实践培训联合创始人
香港中文大学全科预防医学博士
美国抗衰老医学科学院(A4M)认证医师
特别声明
随着解读深入,越来越多的专业词汇,因为翻译时参考资料不同,会出现翻译不当、甚至错误。一者自己会把吃不准的词汇同时标注英文,二者读者要是看到欠妥之处的地方,也欢迎不吝指正,以保证解读信息的准确性。更欢迎大家阅读原版书籍,获得一手信息。
《未完待续》
