周更专栏 | 衰老和积极长寿中基因和基因组
通过2003年完成的人类基因组计划,遗传学和基因组学取得了快速发展。与之形成鲜明对比的是:大多数医生距离真正了解现代遗传学、基因组学及其当前对医学和衰老的影响还很远。虽然科学家对某些过程有着非常精准的了解,但通常离实用医学还很远,有时一些误导有可能对患者是有害的。本章作者在2004年和2021年分别写就了《我们的基因、健康以及我们(Our genes, our Health and We)》和《预测医学的进化(Evolution of Predictive Medicine)》,故此在此话题上有独到的观点。由于涉及一般读者少接触的遗传学专用词汇,所以文末笔者加上了常用的名词解释。
结论
对候选基因、基因组和数百个与长寿相关的多态性位点的测试并没有达到足以预测个体预期寿命的水平。尽管利用新的分子技术寻找衰老的候选基因,也没有突破性的发现,但它提出了许多重要的相关性。基因本身在复杂表型形成中的适度作用,很可能是通过基因间、超分子和细胞间相互作用的复杂机制、调节基因活性的特殊性、客观评估外部因素的真正贡献的困难等来解释的。
当然,遗传在人类健康中所占的比例仅为30%左右,大部分健康是由外部环境因素决定的。不同的外部因素对个体基因组特征的实现,起着决定性的作用。遗传数据如果不考虑患者的生活方式和特征,就一定会导致错误。包括长寿基因在内的基因检测结果只是艰辛的抗衰老工作的开始。只有功能基因组研究而不是静态基因组研究,才能摆脱遗传性缺失和无法正确解释基因检测结果的僵局。
只有通过有针对性的表观遗传效应,纠正减弱的基因变异,充分考虑全基因组的个体特征,才能有望在维持健康寿命和实现最大预期寿命方面取得成功。对个体数据(包括遗传、分子、生活方式等数据)进行综合分析,对于成功的抗衰老干预是必要的。

就已知人类健康和疾病的各种结局都是环境与基因相互作用的结果,遗传因素仅占衰老决定因素的30%~50%。已经有诸多的衰老基因被发现,他们对过早衰老或死亡有着显著意义。所有决定衰老和人类预期寿命的基因,可以分为两大类:生物钟基因和易感基因(也称为薄弱环节基因)[1]。
生物钟基因目前已知有一大群基因,它们参与衰老过程的机制已在实验中得到证实,表1列举了其中的主要基因。
表1:主要的生物钟基因

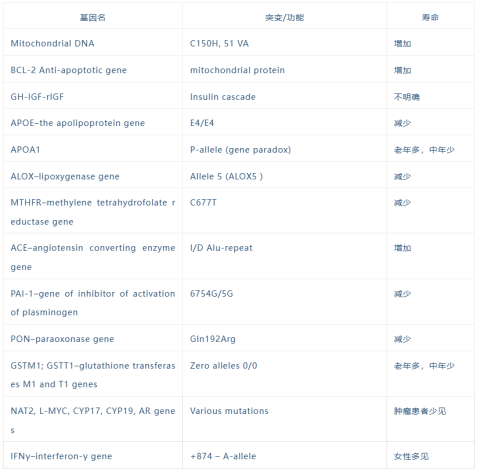
第二类与衰老过程相关的基因是易感基因,又称薄弱环节基因,它与健康寿命的持续时间密切相关,因此也称为“长寿基因”。表2列举了与长寿相关人类基因突变的简要列表。
表2 与长寿相关的人类基因突变
衰老是转录组的进行性退化
表达随年龄显着变化的基因称为年龄调节基因(age regulated genes,ARG)。研究表明,虽然所有ARG都随着年龄超一个方向行动,但不同组织的基因组有所不同,表现为衰老同个体基因有关,而与整个基因组无关。衰老过程中这些ARG活性的减弱会导致细胞功能受到同样的破坏,最终降低整个器官的特定功能。因此,衰老是转录组活性的缓慢下降,是该基因组的功能退化。
已知的数据表明,因为每个人和每个器官都以自己的方式生活和衰老,所以他们及其他们的各器官生物年龄与实际真实年龄也不尽相同。借助功能测试以及实验室检测,可以了解身体各个器官和系统的生物年龄。
抗衰老和积极长寿的方法
衰老遗传学已成为现代老年学和分子医学快速发展的领域。通过改善生活条件质量和对易感基因组进行靶向作用,可以提升功能活性,延缓衰老过程,延长健康寿命。与上述这些目的越来越明显相关的措施包括:
1. 调节长寿基因的活性衰老保护剂(适应原、激素)和生物活性肽(细胞因子)。
2. 中和内毒素(抗氧化剂、螯合剂、复合物)。
3. 通过控制功能缺陷等位基因的表现出现,预防大概率发生的各种多因素疾病(包括衰老)。
现代遗传学开辟了以前无法获得的机会,可以对人类基因组实施有针对性的影响。目前使用的所有老化保护剂以及影响预期寿命的经验因素,都直接或间接地对基因表达有调节作用。因为能直接影响基因活性的保护剂不多,所以更有希望的是通过易感基因的表达调节,实现影响健康质量,因为易感基因的变化会左右各种慢性疾病(包括衰老)的发展。由此,出现的预测医学(predictive medicine),其目的就是早期发现一个人对慢性病的遗传易感性,在症状发生前阶段进行预防,并制定个体化的预防和治疗方法。在之后的章节中,还会提到。
衰老的表观遗传学
衰老过程以及与年龄相关的慢性疾病(衰老疾病)具有典型的多因素性质,即衰老不仅是遗传因素造成的,而且还与调节基因组工作的表观遗传因素有关。
表观遗传调控(变化或紊乱)是衰老过程中基因表达变化的主要原因之一。根据衰老的表观遗传理论,不仅基因突变会随着年龄的增长而积累,而且还会出现许多适应不良的表观遗传变化(表观突变),这些变化会破坏基因的转录并使其工作失去同步。表观遗传变化贯穿一生。它们是稳定的并且可以通过有丝分裂细胞分裂遗传。而且越来越多的证据表明,它们可以跨代遗传,这种表现也出现在人类身上。如祖父在1938年至1939年遭受严重饥荒的丹麦儿童,2 型糖尿病和心血管疾病的发病率显着增加[3]。被围困的列宁格勒的居民也表现出类似的状况[4]。众所周知,幼儿期的生活条件对以后的发育有着长期的影响,直接影响DNA的甲基化。
正如HUGO项目主任弗朗西斯·柯林斯(Francis Collins)所说,“没有人在基因上是完美的,随着基因研究的进展,每个人都可以了解到自己容易患的某种特定疾病[5]。”根据已有的证据,长寿具有显著的遗传性特征,准确的说,遗传因素对长寿的贡献随年龄的增长而逐渐增加[6]。
书中原文还有关于各种衰老理论综述、生物钟基因和易感基因的作用机制,延缓衰老的药物药理,以及一些细节,比如因为缺乏强有力的证据证明端粒长度、健康和人类预期寿命之间的关系,用于人工延长端粒的药物于2012年被正式禁止;又比如众所周知的抗氧化剂有助于小鼠肺部肿瘤的生长,即抗氧化剂具有增强致癌作用,这也和抗氧化剂β胡萝卜素与肺癌患者风险的荟萃分析中得到证实。上述这些非常值得在原书中仔细阅读。
名词解释
基因组学Genome
研究基因表达(活性)如何影响通过环境基因和其他相互作用而改变。
多态性Polymorphism
虽然与突变相同,但多态性在一般人群中的频率要高得多,可以出现50%、60%甚至更多。多态性很常见,也是代表了遗传多样性的体现,这个人的健康和种群的进化是必要的。
参考文献:
[1] Baranova H. Our genes, our Health and We. (Nos gènes, notre santé et nous). Edd. Armand Colin, Paris, Book, 2004. 215 pages
[2] Baranov V.S. et al. Evolution of Predictive Medicine, 2021, EcoVector, S.Pb, Book. 359 pages
[3] Greer E.L., Maures T.J., Ucar D. et al. Transgenerational epigenetic inheritance of longevity in Caenorhabditis elegans // Nature. 2011. Vol. 479. No. 7373. P. 365–371.
[4] Hughes L.A., van den Brandt P.A., de Bruïne A.P. et al. Early life exposure to famine and colorectal cancer risk: a role for epigenetic mechanisms // PLoS One. 2009. Vol. 4. No. 11. P. e7951. doi: 10.1371/journal.pone.0007951.
[5] Collins Fr.S. Shattuck lecture: medical and social consequences of the Human Genome Project. N. Engl. J. Med. 1999. Vol. 341. No. 1. P. 28–37.
[6] Moskalev A.A. Aging and genes. SPb., Nauka, 2008. P. 357.
作 者
Helena Baranova
欧盟“生命科学,生物技术,健康和个性化医学基因组学”委员会专家
欧洲个性化预防与健康研究所(摩纳哥)主席
解读作者
黄力文 Jason LW. Huang
中国抗衰老临床实践培训联合创始人
香港中文大学全科预防医学博士
美国抗衰老医学科学院(A4M)认证医师
《未完待续》
